Вам когда-нибудь доводилось испытывать дискомфорт в животе из-за стресса? Большинство из нас знакомы с этим ощущением, но почему оно возникает? Ученые обнаружили, что оно связано с так называемой осью «кишечник-мозг», то есть с двунаправленным каналом связи между нашим мозгом и кишечником. В течение последних лет нейробиологи и микробиологи уделяли много внимания концепции взаимосвязи мозга и кишечника. Недавно полученные ими данные выявили важную роль в этих процессах и кишечной микробиоты, что позволяет говорить уже об оси «микробиота-кишечник-мозг» [1; 2]. Исследования в данной области начались ещё в конце XIX века, когда было начато изучение взаимосвязей между нашим мозгом и кишечником, а также бактериями, обитающими в кишечнике. Со временем прогресс в исследованиях выявил дополнительные доказательства того, что между этими структурами существуют двунаправленные связи, которые усиливаются во время стресса.
Кишечник иногда называют нашим «вторым мозгом» из-за того, что в нем находятся структуры энтеральной нервной системы (ЭНС) – сети нейронов, которая позволяет кишечнику работать автономно, без инструкций от мозга [3]. ЭНС контролирует работу нашей пищеварительной системы, играет важную роль в перистальтике, секреции и восприятии боли. Наш кишечник является не только «домом» для ЭНС, но и обеспечивает пищей и убежищем комменсальные микроорганизмы – нашу кишечную микробиоту. В настоящее время имеются доказательства того, что кишечник и его микробиота работают сообща, влияя на иммунитет, эндокринные функции, работу кишечника и передачу нервных сигналов.
На рисунках ниже показано схематическое устройство оси «микробиота-кишечник-мозг», а также некоторые патологические состояния, при которых она играет роль
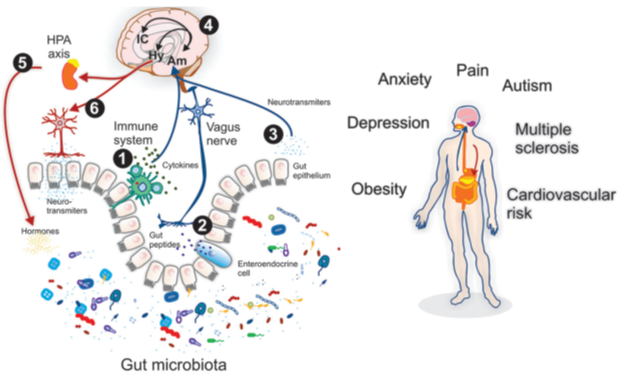
Рисунок А (слева). Ось «микробиота–кишечник–мозг». Прямые и непрямые пути (эндокринные, иммунные и нервные) двунаправленного взаимодействия между микробиотой кишечника и центральной нервной системой. Пути «от кишечника к мозгу» (синие стрелки): (1) лимфоциты получают сигналы из просвета кишечника и выделяют сигнальные молекулы (цитокины), которые оказывают действие на соседние клетки и удалённо; (2) пептидами, выделяемыми энтероэндокринными клетками кишечника, активируют чувствительные окончания блуждающего нерва; (3) микробиота кишечника выделяет нейромедиаторы, которые достигают клетки эпителия кишечника и оказывают влияние на них и удалённо. (4) Нейронные сети в головном мозге, включающие миндалевидное тело (Am) и островковую кору (IC), обрабатывают сигналы от кишечника. Последовательная активация гипоталамуса (Hy) запускает сигнал по пути «от мозга к кишечнику» (красные стрелки): (5) кортикостероиды высвобождаются в результате активации гипоталамо-гипофизарно-надпочечниковой системы (HPA) и модулируют состав микробиоты кишечника; (6) так называемый противовоспалительный холинергический рефлекс и/или симпатическая активация высвобождают нейротрансмиттеры, непосредственно влияющие на состав кишечной микробиоты. Рисунок B (справа). Состояния организма, на которые влияет ось «микробиота-кишечник-мозг». Последние научные данные свидетельствуют о том, что кишечная микробиота через ось «микробиота-кишечник-мозг» может играть роль при некоторых состояниях организма, таких как висцеральная боль, расстройства аутического спектра, ожирение, сердечно-сосудистый риск, тревога/депрессия, рассеянный склероз [Адптировано из 4]
Исследователи обнаружили значительные различия в микробиоте кишечника здоровых людей и пациентов с некоторыми заболеваниями. Судя по имеющимся данным, важное значение имеют как разнообразие, так и относительное изобилие фирмикутов и бифидобактерий. На моделях стерильных животных (не содержащих микроорганизмов) показано, что нормальное и полноценное развитие головного мозга и поведения без нормальной кишечной микробиоты невозможно [5].
Идея использования пробиотиков для улучшения психологического благополучия путём их влияния на ось «микробиота-кишечник-мозг» впервые появилась ещё в XIX веке, но только в начале XXI века эта идея была проверена в доклинических исследованиях на животных и в клинических исследованиях с участием людей. Недавно опубликованный метаанализ 27 исследований с пробиотиками и пребиотиками показал значимое улучшение состояния пациентов при депрессии и тревоге [6]. Важно отметить, что выявленные свойства не являются однородными для всех протестированных пробиотиков, а зависят от конкретных штаммов, что характерно для большинства полезных эффектов пробиотиков.
Какое же влияние оказывают пробиотики на ось «микробиота-кишечник-мозг»? На примере комбинации особых штаммов Lactobacillus helveticus и Bifidobacterium longum было показано, что возможными механизмами действия пробиотиков в данной ситуации являются: уменьшение депрессивного поведения (показано на грызунах); содействие сохранению нормальной нейропластичности и нейрогенеза; предотвращение воспаления в структурах лимбической системы (области мозга, ответственной за реакцию на стресс); поддержание нормального уровня кортизола (у людей и животных); нормализация уровня дофамина и норадреналина в крови (у крыс) и увеличение количества предшественников нейромедиаторов (у крыс и людей); уменьшение апоптоза (нормального процесса программируемой гибели клеток) в головном мозге; поддержание нормальной проницаемости кишечника и уменьшение висцеральной боли; уменьшение воспаления кишечника, вызванного стрессом.
В 2013 году несколько исследователей из Ирландии опубликовали работу «Психобиотики: новый класс психотропных средств», в которой впервые предложили термин «психобиотики» – живые микроорганизмы, которые при попадании в организм в достаточном количестве приносят пользу здоровью пациентов, страдающих психическими заболеваниями [7]. Термин «психобиотики» стали широко использовать для описания пробиотиков, применение которых изучается при депрессии, стрессе, тревоге и других психических расстройствах. Клинические исследования проводят с участием как здоровых лиц, так и пациентов с депрессией, хроническими или нейродегенеративными заболеваниями, такими как болезнь Альцгеймера, аутизм, биполярное расстройство, синдром хронической усталости, мигрень; тревога и депрессия, ассоциированные с синдромом раздражённого кишечника, и другие.
Современные исследования показывают, что воздействие на микробиоту кишечника и ось «микробиота-кишечник-мозг» представляет собой многообещающее направление в неврологии, психологии и психиатрии. Быть может, вскоре использование пробиотиков, пребиотиков и корректировка диеты позволят улучшать качество жизни пациентов и помогут здоровым людям поддерживать свои когнитивные способности, здоровый сон и повышать устойчивость к стрессу.
Литература:
- Wood, J. D. (2007) «Neuropathophysiology of functional gastrointestinal disorders». World Journal of Gastroenterology 13(9): 1313
- Cryan, J. F. And S. M. O’Mahony (2011) «The microbiome-gut-brain axis: from bowel to behavior». Neurogastroenterol Motil 23(3): 187-192
- Liang, S., et al. (2018) «Gut brain psychology: rethinking psychology from the microbiome–gut–brain axis». Frontiers in Integrative Neuroscience12: 33
- Montiel-Castro AJ, et al. The microbiota-gut-brain axis: neurobehavioral correlates, health and sociality. Front Integr Neurosci. 2013 Oct 7;7:70
- Luczynski, P., et al. (2016) «Growing up in a bubble: using germ-free animals to assess the influence of the gut microbiota on brain and behavior». International Journal of Neuropsychopharmacology, 19(8)
- Liu, R. T., et al. (2019) «Prebiotics and probiotics for depression and anxiety: a systematic review and meta-analysis of controlled clinical trials.» Neuroscience & Biobehavioral Reviews, Jul;102:13-23
- Dinan, T. G., C. Stanton and J. F. Cryan (2013) «Psychobiotics: a novel class of psychotropic». Biological Psychiatry 74(10): 720-726