ЧТО ТАКОЕ ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ КИШЕЧНИКА?
Воспалительные заболевания кишечника (ВЗК), к которым относят болезнь Крона (БК) и язвенный колит (ЯК) – это рецидивирующие иммуноопосредованные воспалительные заболевания, при которых наблюдается хроническое воспаление различных отделов желудочно-кишечного тракта (ЖКТ). ВЗК связаны с повышенной активностью иммунной системы ЖКТ, сопровождаются развитием диареи, боли в животе и других кишечных симптомов, а также могут иметь проявления со стороны органов и систем за пределами ЖКТ, включая суставы, органы зрения, кожу и печень.
КАК ЧАСТО ВСТРЕЧАЮТСЯ ВЗК?
ВЗК наиболее распространены в Западной Европе (страдает примерно 1 человек из 1 000) и в Северной Америке (отмечается примерно у 2 человек из 1 000). В Центральной и Южной Европе, Южной Америке, Азии и Африке болеют реже. Однако заболеваемость лиц африканского и латиноамериканского происхождения, проживающих в Северной Америке, более высокая. Чаще всего заболевание дебютирует в возрасте от 20 до 40 лет, второй возрастной пик заболеваемости отмечается в 50-70 лет. Частота развития ВЗК у мужчин и женщин существенно не различается [1; 2].
ЧЕМ ОТЛИЧАЮТСЯ МЕЖДУ СОБОЙ БОЛЕЗНЬ КРОНА И ЯЗВЕННЫЙ КОЛИТ?
Несмотря на сходство симптомов, БК и ЯК имеют характерные особенности.
Так при БК поражается любой отдел ЖКТ, но преимущественно тонкая кишка, с образованием фистул (свищей), объёмных образований и абсцессов (гнойников); прямая кишка обычно не поражается, выделение крови из прямой кишки (за исключением случаев колита) наблюдается редко. Характерные данные отмечаются при проведении инструментальных исследований – рентгенографии кишечника, колоноскопии, гистологическом исследования участков кишечника.
ЯК поражает только толстую кишку, всегда поражает прямую кишку, из которой отмечается выделение крови. А вот образование фистул в кишке не наблюдается. Инструментальные исследования также выявляют характерные изменения [3].
КАК ПРОЯВЛЯЮТСЯ ВЗК ЗА ПРЕДЕЛАМИ КИШЕЧНИКА?
Большинство внекишечных проявлений значительно чаще наблюдаются при ЯК и БК с вовлечением толстой кишки (с колитом), чем при БК без колита. Отмечают поражения суставов (периферический артрит крупных суставов, анкилозирующий спондилит, сакроилеит), глаз (эписклерит, увеит), кожи (узловатая эритема, гангренозная пиодермия), слизистой оболочки полости рта (афтозный стоматит), печени (желчнокаменная болезнь, склерозирующий холангит, перихолангит, цирроз, аутоиммунный гепатит), почек (мочекаменная болезнь, гидронефроз).
При тяжёлом течении ВЗК, а также после оперативных вмешательств по поводу ВЗК может развиться мальабсорбция – нарушение всасывания питательных веществ, макро- и микроэлементов, витаминов – она может приводить к их дефициту и проявляться анемией, снижением содержания кальция и магния в крови, нарушениями свертывания крови, деминерализации костной ткани. У детей мальабсорбция может сопровождаться задержкой роста и развития.
Также могут развиваться тромбоэмболические осложнения и амилоидоз (на фоне длительно текущего воспалительного и гнойного процесса) [3].
КАКОВЫ ПРИЧИНЫ РАЗВИТИЯ ВЗК?
Причины возникновения ВЗК точно не известны. Факторами риска являются генетическая предрасположенность, а также экологическая обстановка, особенности питания, состояние иммунной системы и микробиоты кишечника, например, отсутствие достаточного контакта с микроорганизмами в детстве из-за чрезмерной гигиены (см. Рисунок 1). Если среди родственников 1-й степени родства есть пациенты с ВЗК, то риск заболеть повышается в 4-20 раз. Семейная предрасположенность значительно более выражена при БК, чем при ЯК. Обнаружено несколько генетических мутаций, лежащих в основе предрасположенности к ВЗК [4; 5]. Предполагают, что курение способствует обострению БК, но снижает риск развития ЯК. Аппендэктомия, применяемая для лечения острого аппендицита, также снижает риск возникновения ЯК. Приём нестероидных противовоспалительных препаратов (НПВП), оральных контрацептивов может увеличивать риск развития БК. Некоторые данные позволяют предположить, что использование антибиотиков в детском возрасте может быть связано с повышенным риском возникновения ВЗК [6].
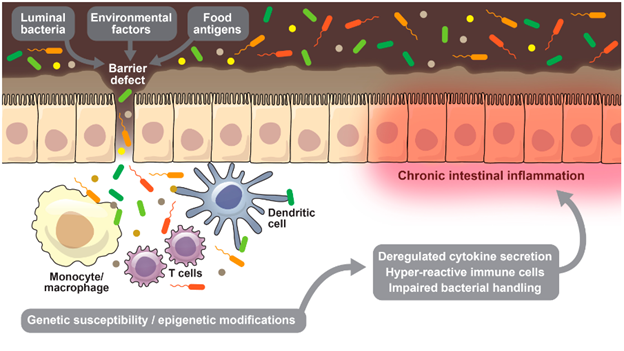
Рисунок 1. Современная гипотеза патогенеза ВЗК. Микробиота кишечника, факторы окружающей среды и пищевые антигены нарушают целостность кишечного барьера и проникают через него в более глубокие слои подслизистой ткани. В генетически восприимчивом организме происходят эпигенетические модификации и нарушение регуляции врожденного и адаптивного иммунного ответа. В конечном итоге это проявляется воспалением кишечника [Адаптировано из 7].
КАКОВА РОЛЬ КИШЕЧНОЙ МИКРОБИОТЫ В РАЗВИТИИ ВЗК?
Микробиота кишечника играет важную, но все еще слабо понимаемую роль в развитии ВЗК. В многочисленных исследованиях у пациентов с ВЗК наблюдают дисбиоз, т. е. нарушение равновесия, структуры и функции микробиоты, отмечают снижение численности бактерий, обладающих противовоспалительной активностью – этот дисбаланс может вызывать и поддерживать хроническое воспаление кишечника [8; 9].
КАК ЛЕЧАТ ВЗК?
Пациентам и членам их семей предоставляется информация, касающаяся диеты и поведения в стрессовых ситуациях. Хотя имеются отдельные сообщения об улучшении состояния при соблюдении определенных диет, например, с жестким ограничением углеводов, в контролируемых исследованиях убедительные преимущества такого питания не доказаны. Устранение стрессовых ситуаций оказывает благоприятный эффект.
Радикальное лечение ВЗК не разработано, но лекарственная терапия может облегчить болезненные обострения. Применяют следующие препараты: 5-аминосалициловая кислота; кортикостероиды; иммуномодуляторы; биологические лекарственные препараты (моноклональные антитела-антицитокиновые препараты); низкомолекулярные таргетные базисные провоспалительные препараты (например, ингибиторы янус-киназы, модуляторы рецепторов сфингозин-1-фосфата); в ряде случаев – антибиотики (например, метронидазол, ципрофлоксацин) и пробиотики.
Примерно в 80% случаев при БК и в 20% при ЯК требуется проведение хирургического лечения. В редких случаях оно приводит к окончательному выздоровлению [3].
КАКОВО ЗНАЧЕНИЕ ВМЕШАТЕЛЬСТВ, НАПРАВЛЕННЫХ НА МИКРОБИОТУ, ПРИ ЛЕЧЕНИИ ВЗК?
В настоящее время исследователи, учитывая возможную роль патогенезе ВЗК кишечной микробиоты, разрабатывают вмешательства, нацеленные на неё [10]. Так дополнительное включение некоторых пробиотиков в состав стандартной терапии ВЗК способствует уменьшению дисбиотических проявлений благодаря подавлению «агрессивных» бактериальных видов и восстановлению «полезных» видов, оказывает положительное иммунорегуляторное воздействие, увеличивая функциональную активность иммунокомпетентных клеток без снижения активности гуморального иммунитета, способствует снижению уровня циркулирующих иммунных комплексов (см. Рисунок 2) [11].

Рисунок 2. Основные предполагаемые механизмы действия пробиотиков при ВЗК [Адаптировано из 12].
КАКИЕ РЕЗУЛЬТАТЫ ПОЛУЧЕНЫ В КЛИНИЧЕСКИХ ИССЛЕДОВАНИЯХ ПРОБИОТИКОВ ПРИ ВЗК И ЧТО ОБ ЭТОМ ГОВОРЯТ ЭКСПЕРТЫ?
В нескольких систематических обзорах клинических исследований продемонстрированы эффекты пробиотиков по индукции и поддержанию ремиссии ЯК, а также паучита (воспаление хирургически сформированного резервуара после операции на толстой кишке), но отмечено, что данные об эффектах пробиотиков при БК неубедительны. Необходимо дальнейшее изучения эффективности и безопасности пробиотиков для понимания их места в комплексной терапии и вторичной профилактике ЯК [13-16].
В обновлённых рекомендациях Всемирной организации гастроэнтерологов по пробиотикам и пребиотикам отмечается возможность применения определённых штаммов пробиотиков и их комбинаций для вспомогательной терапии и профилактики паучита, индукции и поддержания ремиссии ЯК [17].
Если вы или ваши близкие страдаете ЯК, посоветуйтесь с вашим гастроэнтерологом о возможности включения определённых пробиотиков в схему терапии и профилактики обострений данного заболевания.
ВЫПОЛНЯЮТ ЛИ ПРИ ВЗК ТРАНСПЛАНТАЦИЮ ФЕКАЛЬНОЙ МИКРОБИОТЫ?
Ещё одной из технологий, нацеленных на микробиоту кишечника, которая сейчас активно изучается в клинических исследованиях при ВЗК, является трансплантация фекальной микробиоты (ТФМ). ТФМ – это введение особым образом обработанной и подготовленной фекальной суспензии, полученной от здоровых доноров, в ЖКТ пациентов с целью восстановления стабильной кишечной микробиоты. Обнадеживающие результаты получены при использовании ТФМ для лечения ЯК [18]. Относительно применения ТФМ при БК пока не существует единого мнения, однако необходимость коррекции микробиоты ЖКТ ни у кого не вызывает сомнений. На это направлены проводимые клинические исследования, которые позволят лучше понять значение и место вмешательств, нацеленных на микробиоту при ВЗК, включая ТФМ [19].
Литература:
- Bernstein CN, Rawsthorne P, Cheang M, et al: A population-based case control study of potential risk factors for IBD. Am J Gastroenterol 101(5):993-1002, 2006
- Schiff ER, Frampton M, Semplici F, et al: A new look at familial risk of inflammatory bowel disease in the Ashkenazi Jewish population. Dig Dis Sci 63(11):3049-3057, 2018
- Aaron E. Walfish and Rafael Antonio Ching Companioni, Overview of Inflammatory Bowel Disease, rev. November 2023
- Halfvarson J, Bodin L, Tysk C, et al. Inflammatory bowel disease in a Swedish twin cohort: a long-term follow-up of concordance and clinical characteristics. Gastroenterology. 2003;124(7):1767-1773
- Gent AE, Hellier MD, Grace RH, et al. Inflammatory bowel disease and domestic hygiene in infancy. Lancet. 1994;343(8900):766-767
- Cosnes J, Gower-Rousseau C, Seksik P, et al. Epidemiology and natural history of inflammatory bowel diseases. Gastroenterology. 2011 May;140(6):1785-94
- Rogler G, Biedermann L, Scharl M. New insights into the pathophysiology of inflammatory bowel disease: microbiota, epigenetics and common signalling pathways. Swiss Med Wkly. 2018 Mar 22;148:w14599
- Frank DN, St Amand AL, Feldman RA, et al. Molecular-phylogenetic characterization of microbial community imbalances in human inflammatory bowel diseases. Proc Natl Acad Sci U S A. 2007;104(34):13780-13785
- Manichanh C, Rigottier-Gois L, Bonnaud E, et al. Reduced diversity of faecal microbiota in Crohn’s disease revealed by a metagenomic approach. Gut. 2006;55(2):205-211
- Bejaoui M, Sokol H, Marteau P. Targeting the Microbiome in Inflammatory Bowel Disease: Critical Evaluation of Current Concepts and Moving to New Horizons. Dig Dis. 2015;33 Suppl 1:105-112
- Ситкин С.И., Орлова Н.А. Воспалительные заболевания кишечника. Возможности и перспективы современной фармакотерапии. Гастроэнтерология Санкт-Петербурга. 2006; 3: 2–8
- М.Ф. Осипенко, М.И. Скалинская, А.А. Размерица. Пробиотики и воспалительные заболевания кишечника. Consilium Medicum. Гастроэнтерология (Прил.). 2013; 2: 28-32
- Ghouri YA, et al. Systematic review of randomized controlled trials of probiotics, prebiotics, and synbiotics in inflammatory bowel disease. Clin Exp Gastroenterol. 2014 Dec 9;7:473-87
- Derwa Y, et al. Systematic review with meta-analysis: the efficacy of probiotics in inflammatory bowel disease. Aliment Pharmacol Ther. 2017 Aug;46(4):389-400
- Zhang XF, et al. Clinical effects and gut microbiota changes of using probiotics, prebiotics or synbiotics in inflammatory bowel disease: a systematic review and meta-analysis. Eur J Nutr. 2021 Aug;60(5):2855-2875
- Kaur L, et al. Probiotics for induction of remission in ulcerative colitis. Cochrane Database Syst Rev. 2020 Mar 4;3(3):CD005573
- Guarner F, et al. World Gastroenterology Organisation Global Guidelines: Probiotics and Prebiotics. J Clin Gastroenterol. 2024 Jul 1;58(6):533-553
- Moayyedi P., Surette M.G., Kim P.T., et al. Fecal microbiota transplantation induces remission in patients with active ulcerative colitis in a randomized controlled trial. Gastroenterol. 2015; 149(1): 102–109
- Евдокимова Н.В., Черненькая Т.В. Трансплантация фекальной микробиоты: прошлое, настоящее и будущее. Журнал им. Н.В. Склифосовского Неотложная медицинская помощь. 2019; 8(2): 160-165